编者按:2021欧洲心脏病学会(ESC)年会Late Breaking Science in Arrhythmias公布了三项最新科学研究,本刊特邀上海交通大学附属胸科医院何奔教授团队进行专题点评,与您一同深入学习。
房颤患者的卒中风险显著升高,随着循证医学证据的不断更新,经皮左心耳封堵术(Left atrial appendage closure, LAAC)作为口服抗凝药(Oral anticoagulation, OAC)的替代,在非瓣膜性房颤患者,尤其是不耐受或不愿意使用OAC以及高出血风险人群的卒中预防方面正扮演着愈发重要的角色。
目前,临床上可供选择的经皮左心耳封堵器械主要包括塞式和盖式两大类。其中,塞式封堵器的代表是美国波士顿科学公司的Watchman封堵器,在PROTECT-AF及PREVAIL等随机对照研究(Randomized controlled trial, RCT)证据的支持下,于2013年经美国食品药品监督管理局(FDA)批准用于临床,迄今全球植入例数已超过10万例,改良后的二代产品Watchman FLX也于2020年7月获得FDA审批。
与之相比,盖式封堵器产品众多,包括ACP、Amulet及国产LAmbre、LAcBes等均已在临床广泛应用。但由于缺乏RCT研究结果,基本都仅获得欧盟CE认证,尚未取得FDA审批。2021年8月16日,雅培公司宣布其自主研制的Amplatzer Amulet左心耳封堵器正式获得FDA批准,其关键证据正是来自Amulet IDE研究。该研究结果刚刚于欧洲心脏病学会议(ESC 2021)上公布,让我们来一睹为快。
研究背景
Amulet封堵器是雅培公司在其一代产品ACP基础上改良研发的新一代盖式封堵器,遵循内固定盘+外封堵盘的设计理念(Pacifier principle),两者通过凹陷的腰部相连。Amulet封堵器的内盘尺寸为16~34mm,外盘尺寸22~41mm,可适应不同大小的左心耳。(图1)
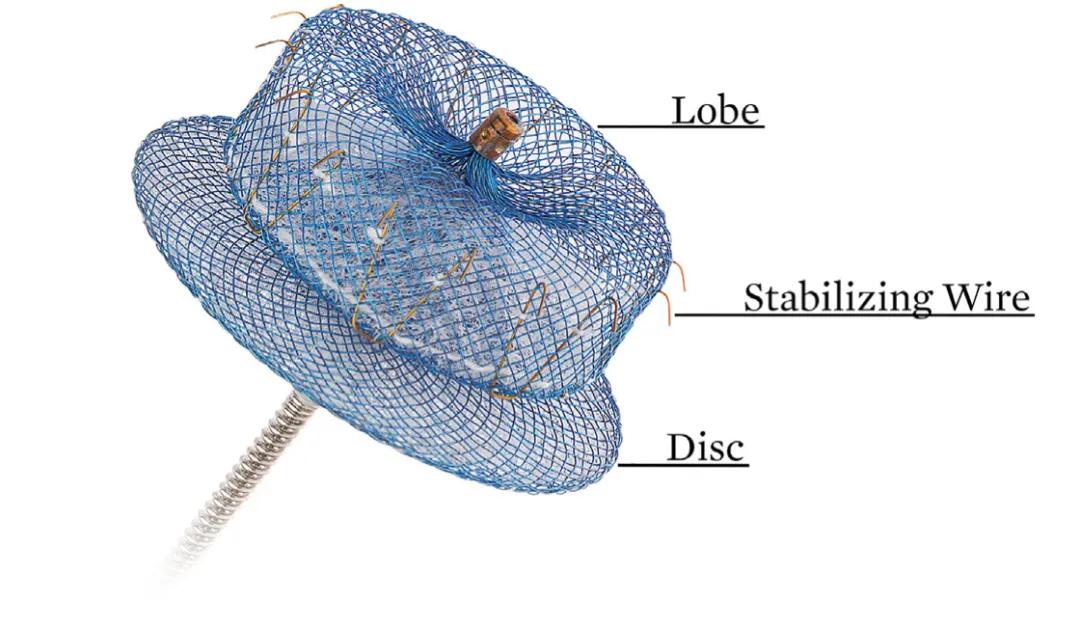
图1 Amulet封堵器设计
2018年公布的一项Amulet封堵器单臂观察性研究中,来自17个国家的1088名高危房颤患者接受了Amulet左心耳封堵术,手术成功率达到99.0%,围术期并发症发生率3.2%。术后平均67±23天的食道超声(Tranesophageal echocardiography, TEE)随访结果显示,有效封堵率达到98.2%,器械相关血栓(Device-related thrombosis, DRT)的发生率仅1.5%。在早期临床应用经验的基础上,Amulet IDE研究拟通过与Watchman封堵器的头对头比较,评价Amulet封堵器在预防房颤卒中方面的安全性和有效性。
研究方法
Amulet IDE是一项前瞻性、多中心、随机对照研究,计划纳入来自全球150家中心的1878名卒中高危(CHADS2评分≥2分或CHA2DS2-VASc评分≥3分)非瓣膜性房颤患者,1:1随机分入Amulet或Watchman封堵器组。术前需服用阿司匹林(81~100mg),对于已接受OAC治疗的患者可继续服用无需桥接。手术可在局麻或全麻下进行,但必须经TEE和造影指导,术中造影确认着陆区宽度在11~31mm,心耳深度在10mm以上。
两组患者的术后抗栓方案不同。术后45天内,Amulet组患者接受双联抗血小板(Dual antiplatelet therapy, DAPT)或阿司匹林+OAC治疗,Watchman组患者接受阿司匹林+华法林治疗。如果45天的TEE复查未发现显著残余分流(>5mm),则两组均改为DAPT抗栓至术后6月,然后切换至长期阿司匹林单抗。有显著残余分流的患者继续接受阿司匹林+OAC治疗。如果任何时间发现DRT,则启动4~6周的华法林抗凝及后续的TEE复查。术后随访期为5年。(图2)
研究共有3个主要终点,分别用于评价Amulet封堵器的安全性、有效性和封堵机制。主要安全性终点是手术相关并发症、12个月内的全因死亡或大出血(BARC≥3型)的复合终点。主要有效性终点包括18个月内的缺血性卒中或系统性栓塞。评价封堵机制的主要终点是45天随访时的有效封堵率(有效封堵指TEE下残余分流≤5mm)。研究还有5个次要终点。每个主要终点(非劣效性)都设有相应的次要终点(优效性),此外,Amulet组术后18个月内的所有卒中、系统性栓塞、心血管或不明原因的死亡组成的复合终点的非劣效性以及大出血事件发生率(BARC≥3型)的优效性也是研究的次要终点。
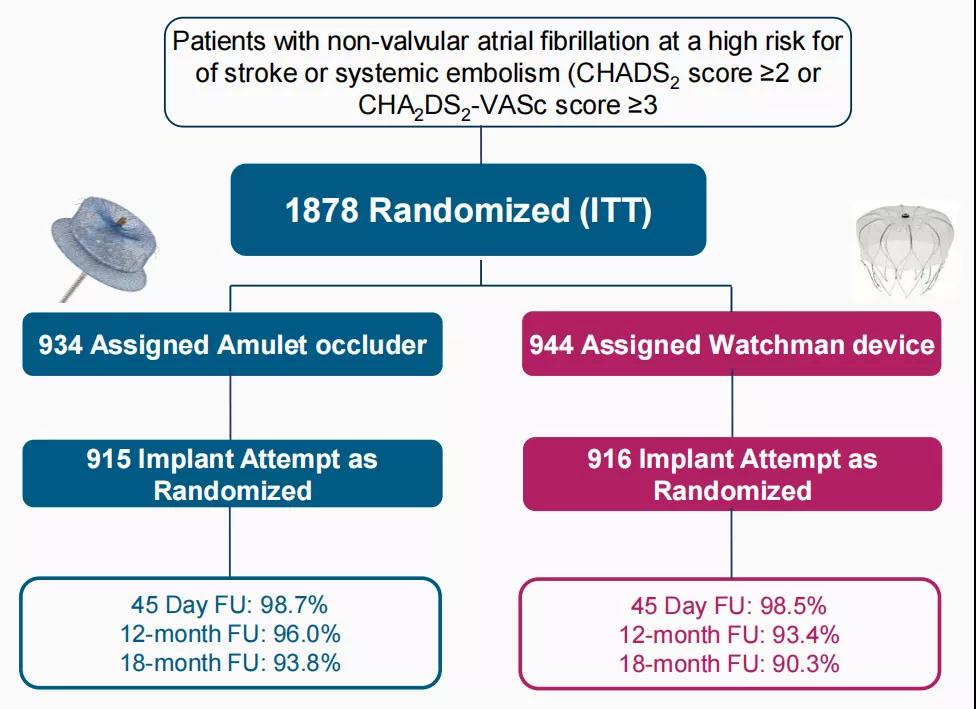
图2 研究流程图
研究结果
Amulet IDE研究共入组1878例患者,最终实际根据随机结果接受封堵治疗的患者共1831例,其中Amulet组915例,Watchman组916例。两组术后45天的随访率分别达98.7%和98.5%,术后18个月随访率也均在90%以上。
研究的三个主要终点均达到非劣效性结果。其中,两组的主要有效性终点(术后18个月)发生率分别为2.8% vs 2.8%(Amulet vs Watchman,p<0.001),主要安全性终点(术后12个月)分别为14.5%和14.7%(p=0.0002)。此外,评价封堵机制的有效封堵率分别为98.9%和96.8%(p<0.0001),同时还达到了优效性终点(p=0.0025)。(图3)

图3 主要研究终点
术后抗栓治疗策略方面,Amulet组抗血小板或未用抗栓治疗的患者比例高达78.9%,抗凝患者仅占21.1%;而绝大多数(95.8%)的Watchman组患者均接受了抗凝治疗,抗板或未用抗栓药物的患者仅占4.2%。(图4)

图4 术后抗栓策略
研究结论
Amulet左心耳封堵器在房颤患者卒中预防中安全有效,且术后可能无需抗凝治疗。
研究点评
Amulet IDE研究是一项全球范围的前瞻性、多中心、随机对照研究,通过与Watchman封堵器的头对头比较,评价Amulet封堵器在房颤卒中预防方面的安全性和有效性。结果显示,3个非劣效性主要终点全部达到,提示Amulet封堵器在房颤患者卒中预防中安全有效,且术后多数患者可无需抗凝治疗。在此之前,LAAC的RCT研究证据仅来自Watchman这一种塞式封堵器(PROTECT-AF、PREVAIL等),作为盖式封堵器的代表,Amulet的这项头对头RCT研究结果,无疑进一步夯实了LAAC能安全有效预防房颤卒中的循证医学证据,也为盖式封堵器的临床应用提供了有力支撑。
笔者认为,该研究主要有以下几点值得关注:
(1)术后18个月缺血性卒中或系统性栓塞的有效性终点上,Amulet组事件率仅为2.8%,与Watchman相当,由于入组的均为卒中高危患者,可见血栓风险显著降低,LAAC对房颤卒中预防的效力毋庸置疑。
(2)安全性终点包括了手术相关并发症、12个月内的全因死亡或大出血事件(BARC≥3型),两组并无显著差异。但由于全部研究结果尚未发表,无法明确各类安全终点的发生情况。手术相关并发症(如心包填塞、器械脱落等)对于评价一款封堵器的安全性至关重要。盖式封堵器对心耳深度的要求较小,理论上因封堵器头端刺破心耳尖部引起心包填塞的概率更低,但同时在临床实践中观察到盖式封堵器存在一定迟发心包积液(Late pericardial effusion, LPE)的情况,其发生率与机制也有待进一步探讨明确。此外,Watchman二代产品Watchman FLX的初步应用结果PINNACLE FLX也已发表在今年5月的Circulation杂志上,1年随访安全性事件发生率仅为0.5%,较PREVAIL、CAP/CAP2中一代产品的安全性事件率显著降低,一方面反映了LAAC手术安全性的不断提高,同时也对其他产品及后续改良提出了更高的安全要求。
(3)研究针对两款封堵器的不同封堵理念和设计特点,特设了通过残余分流(≤5mm)评价封堵机制的主要终点,结果显示Amulet优于Watchman封堵器,残余分流发生率更低。残余分流形成的根部原因在于统一设计的封堵装置不能个性化匹配心耳复杂多变的形态,从这一机制来说,Amulet装置双盘+腰部连接的设计往往能使封堵器与心耳更好地匹配贴合,同时内外盘均含有利于封堵的聚酯材料,也提高了有效封堵率。但PROTECT-AF研究定义Watchman装置5 mm以内的残余分流均属于成功封堵,既往随机和注册研究结果没有发现残余分流与血栓或MACE事件相关,因此残余分流减少是否足以成为盖式封堵器的优势仍有待论证。此外,PINNACLE FLX研究中1年随访有90%的患者没有发现残余分流,而在早期的PROTECT-AF和PREVAIL研究中这一数据仅为66%,残余分流的比例也已大幅缩小,同时没有观察到>5mm的显著残余分流。
研究的另一亮点在于,Amulet组术后大部分(78.9%)患者均未服用抗凝药,相比之下,Watchman组抗凝治疗的比例则高达95.8%。由于尚未公布DRT发生率,考虑到两组在主要终点事件上并无显著差异,可能提示Amulet术后直接停用抗凝治疗是可行的。但另一方面,目前Watchman的术后标准抗栓方案(华法林+阿司匹林)仍是基于早期PROTECT-AF和PREVAIL研究,本研究中Watchman组也主要采用这一抗栓方案。但事实上,随着新型口服抗凝药(Novel anticoagulant, NOAC)的兴起,临床上LAAC术后已更多采用NOAC抗凝甚至抗血小板治疗,ASAP等注册研究也提示Watchman术后使用抗血小板治疗安全有效。同时从装置特点来看,与Watchman相比,Amulet等盖式封堵器也并不存在能减少DRT的设计特点。因此,现阶段仍建议根据患者的血栓和出血风险,个性化制定LAAC术后的抗栓策略,加强影像学随访,做好术后管理,使患者真正获益。
Amulet IDE研究首次为盖式封堵器“正名”,也从器械层面进一步丰富了LAAC的循证医学证据。近两年来,包括PRAGUE-17、LAAOS-III在内的多个LAAC的RCT研究结果陆续出炉,左心耳封堵正经历日新月异的变化。期待更多高质量临床研究结果的公布能不断助力LAAC的蓬勃发展,也预祝中国左心耳封堵的优秀研究和器械能借其东风,鹏程万里。
专家简介
何奔教授
上海交通大学附属胸科医院心脏中心主任医师,博士生导师,二级教授现任上海市胸科医院心脏中心主任,心血管内科主任,上海市领军人才,上海市优秀学科带头人,卫生部有突出贡献中青年专家, 获国务院特殊津贴。曾获上海交通大学校长奖,上海市十佳医生,上海市五一劳动奖章,中国十大口碑医生等荣誉。擅长各种复杂冠脉介入治疗以及结构性心脏病的介入治疗,是上海首位全球标准认定的左心耳封堵术培训导师。对各种危重疑难心血管疾病的诊治有较高的造诣。学术任职:中华医学会心血管病学分会全国常委,中国心血管医师协会全国常委,上海市心血管病学会副主任委员,美国心脏学会专家会员,欧洲心脏学会专家会员。
 京公网安备 11010502033353号 增值电信业务经营许可证:京ICP证150541号
京公网安备 11010502033353号 增值电信业务经营许可证:京ICP证150541号